Bonding in General Organic Chemistry (सामान्य कार्बनिक रसायन में बंधन)
In organic chemistry, bonding explains how atoms connect to form molecules. Most organic compounds involve covalent bonds between C, H, O, N, and halogens. कार्बनिक रसायन में, बंधन यह समझाता है कि परमाणु आपस में कैसे जुड़ते हैं। अधिकांश कार्बनिक यौगिक सहसंयोजक बंधनों से बने होते हैं।
1. Types of Covalent Bonds (सहसंयोजक बंधों के प्रकार)
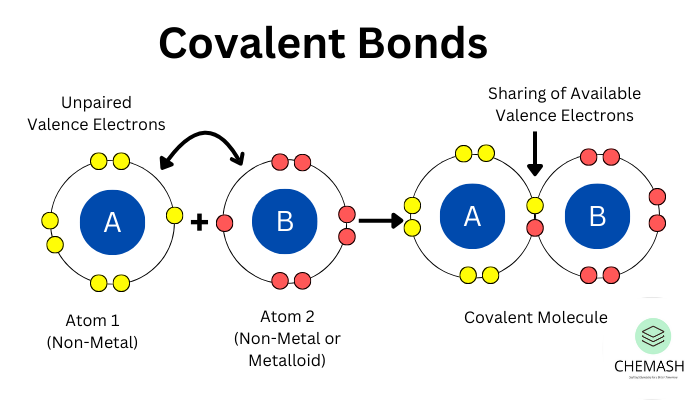
- Single Bond (σ bond): Head-on overlap. Example: C–C in ethane.
एकल बंध: σ बंध का निर्माण अग्रिम ओवरलैप से होता है। - Double Bond: One σ + one π bond. Example: C=C in ethene.
द्वि-बंध: एक σ और एक π बंध से मिलकर। - Triple Bond: One σ + two π bonds. Example: C≡C in ethyne.
त्रि-बंध: एक σ और दो π बंध से मिलकर।
2. Hybridization (संकरण)
| Hybridization | Geometry | Bond Angle | Example |
|---|---|---|---|
| sp³ | Tetrahedral | 109.5° | CH₄ (Methane) |
| sp² | Trigonal Planar | 120° | C₂H₄ (Ethene) |
| sp | Linear | 180° | C₂H₂ (Ethyne) |
3. Bond Length & Bond Strength (बंधन लंबाई और शक्ति)
- Bond length decreases: C–C > C=C > C≡C
- Bond strength increases from single → triple bond
4. Resonance (अनुनाद)
Benzene (C₆H₆) shows resonance → equal bond lengths. बेंजीन में सभी C–C बंध समान लंबाई के होते हैं।
5. Polar & Nonpolar Bonds
Polar → unequal electron sharing (C–O). Nonpolar → equal sharing (C–C, C–H). ध्रुवीय बंध: असमान इलेक्ट्रॉन साझाकरण। अध्रुवीय: समान साझाकरण।
6. Molecular Orbitals (आणविक कक्षाएँ)
Combination of orbitals → bonding & antibonding MOs. Explains aromaticity & conjugation. आणविक कक्षाएँ संयुग्मन और सुगंधता को समझाती हैं।
7. Electron Displacement Effects
- Inductive Effect (–I/+I)
- Resonance Effect (–R/+R)
- Hyperconjugation
- Electromeric Effect
8. Aromaticity
Benzene follows Huckel’s Rule (4n+2 π electrons). बेंजीन में 6 π इलेक्ट्रॉन्स → सुगंधता।
MCQs
- Which bond is formed by end-to-end overlap? → σ bond
- Hybridization of carbon in ethene? → sp²
- Shortest bond length? → C≡C
True/False
- Triple bonds are longer than single bonds. → False
- Benzene has equal bond lengths. → True
Fill in the Blanks
1. sp³ hybridization gives ______ geometry. → Tetrahedral
FAQ
Q1: Why is resonance important?
Ans: Resonance stabilizes molecules by delocalization of π electrons.
Q2: What is hyperconjugation?
Ans: Delocalization of σ electrons of C–H bond with adjacent π system.

Pingback: Isomerism in Organic Chemistry: Types, Examples & Quiz - CHEMASH